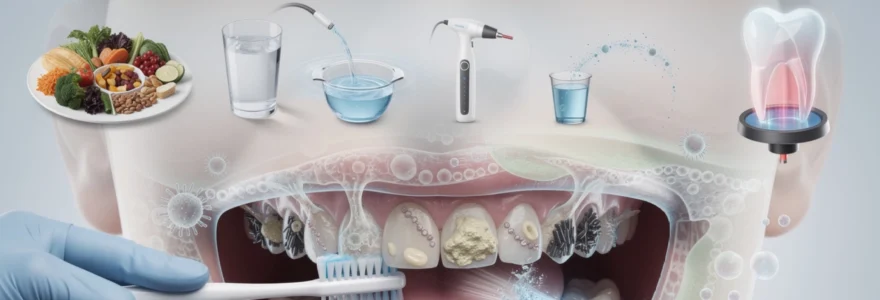
La cavité buccale constitue un véritable écosystème microbien où cohabitent plus de 700 espèces bactériennes différentes. Cette diversité microbienne, bien que naturelle, peut devenir problématique lorsque l’équilibre entre bactéries bénéfiques et pathogènes se rompt. Les conséquences d’un déséquilibre du microbiote oral s’étendent bien au-delà de la simple mauvaise haleine, pouvant engendrer des caries, des maladies parodontales et même des complications systémiques affectant le système cardiovasculaire. Comprendre les mécanismes de protection de la cavité buccale contre les bactéries pathogènes devient donc essentiel pour maintenir une santé bucco-dentaire optimale et prévenir les infections orales.
Microbiome buccal et écosystème pathogène : comprendre la flore microbienne
Le microbiome buccal représente l’un des écosystèmes microbiens les plus complexes du corps humain. Cette communauté microbienne dynamique fluctue constamment en fonction de nombreux facteurs environnementaux, nutritionnels et comportementaux. La salive joue un rôle fondamental dans la régulation de cet écosystème, maintenant un pH neutre et fournissant des nutriments essentiels aux micro-organismes bénéfiques. L’équilibre délicat de ce microbiome détermine largement la susceptibilité aux infections et aux maladies bucco-dentaires.
Les bactéries commensales, telles que les Streptococcus sanguinis et les Actinomyces, occupent des niches écologiques spécifiques et créent une barrière protectrice contre les pathogènes opportunistes. Ces micro-organismes bénéfiques produisent des substances antimicrobiennes naturelles et consomment les nutriments disponibles, limitant ainsi la croissance des espèces pathogènes. La diversité microbienne constitue un facteur clé de résistance aux infections, car un microbiome riche et varié offre une protection plus efficace qu’un écosystème appauvri.
Streptococcus mutans et formation du biofilm dentaire
Streptococcus mutans représente l’agent pathogène principal responsable de la formation de caries dentaires. Cette bactérie acidogène possède une capacité remarquable à adhérer aux surfaces dentaires et à métaboliser les sucres alimentaires en acide lactique. Le processus de formation du biofilm débute par l’adhésion initiale des bactéries aux protéines salivaires adsorbées sur l’émail dentaire, créant une pellicule acquise qui facilite la colonisation microbienne.
La production d’exopolysaccharides par S. mutans permet la formation d’une matrice extracellulaire protectrice qui rend le biofilm résistant aux agents antimicrobiens et aux forces de cisaillement de la salive. Cette matrice complexe crée un environnement acidique localisé où le pH peut descendre jusqu’à 4,5, provoquant la déminéralisation de l’émail dentaire. La virulence de cette bactérie réside dans sa capacité à survivre dans des conditions acides extrêmes et à continuer sa production d’acides même en présence de concentrations élevées de sucrose.
Porphyromonas gingivalis et pathogenèse parodontale
Porphyromonas gingivalis constitue l’un des pathogènes parodontaux les plus virulents, souvent qualifié de « pierre ang
gulaire » de la dysbiose parodontale. Anaérobie stricte, elle colonise préférentiellement les poches parodontales profondes, où l’oxygène est quasi absent et où la plaque sous-gingivale s’accumule. P. gingivalis sécrète des protéases puissantes, les gingipaïnes, capables de dégrader le collagène, les immunoglobulines et les protéines de la matrice extracellulaire, favorisant ainsi la destruction progressive des tissus de soutien de la dent.
Au-delà de son action locale, cette bactérie module la réponse immunitaire de l’hôte en perturbant l’équilibre entre cytokines pro-inflammatoires et anti-inflammatoires. Elle agit comme un « pathogène clé de voûte », modifiant l’environnement microbien et ouvrant la voie à d’autres bactéries parodontopathogènes. La présence élevée de P. gingivalis est associée à un risque accru de parodontite chronique, mais aussi à des pathologies systémiques, notamment les maladies cardiovasculaires et certains troubles métaboliques.
Candida albicans et infections fongiques orales
Candida albicans est une levure commensale de la cavité buccale, généralement contrôlée par le système immunitaire et la compétition avec les bactéries bénéfiques. Toutefois, en cas d’immunodépression, de sécheresse buccale ou de prise prolongée d’antibiotiques, cette levure peut proliférer et provoquer une candidose orale. Cette infection fongique se manifeste par des dépôts blanchâtres sur la langue, le palais ou l’intérieur des joues, souvent associés à des brûlures ou une gêne lors de la déglutition.
La capacité de C. albicans à passer d’une forme levuriforme à une forme filamenteuse (hyphes) constitue un facteur majeur de virulence. Cette transition morphologique lui permet de pénétrer les tissus muqueux et de former des biofilms mixtes avec certaines bactéries comme Streptococcus mutans. Ces biofilms fongo-bactériens sont particulièrement résistants aux traitements classiques et contribuent au développement de caries rampantes chez les patients fragilisés. Préserver un microbiote buccal équilibré et une immunité salivaire efficace reste donc essentiel pour limiter l’émergence de ces infections fongiques.
Fusobacterium nucleatum et halitose chronique
Fusobacterium nucleatum est une bactérie anaérobie fréquemment impliquée dans l’halitose chronique. Installée dans les espaces interdentaires, les poches gingivales et sur le dos de la langue, elle dégrade les protéines salivaires et les débris alimentaires en composés sulfurés volatils (CSV). Ce sont ces molécules, comme le sulfure d’hydrogène et le méthylmercaptan, qui sont responsables de la mauvaise haleine persistante malgré un brossage apparemment correct.
Au-delà de la gêne sociale, la prolifération de F. nucleatum traduit souvent un déséquilibre du microbiote oral et une hygiène bucco-dentaire insuffisante, en particulier au niveau de la langue. Des études récentes suggèrent également un rôle potentiel de cette bactérie dans certaines pathologies extra-buccales, notamment des complications respiratoires et des infections systémiques. Une prise en charge globale de l’halitose, incluant nettoyage lingual, contrôle de la plaque et assainissement parodontal, s’avère donc indispensable pour rétablir un environnement buccal sain.
Techniques de décontamination mécanique et chimique de la cavité buccale
Protéger sa cavité buccale des bactéries pathogènes repose sur une combinaison de méthodes mécaniques et chimiques, appliquées de façon régulière et rigoureuse. Vous pouvez imaginer cette stratégie comme un double bouclier : le premier, mécanique, vise à désorganiser le biofilm et à éliminer physiquement la plaque ; le second, chimique, cible les micro-organismes résiduels et module la flore microbienne. L’enjeu n’est pas de stériliser la bouche, mais d’orienter le microbiote vers un état compatible avec la santé.
Une technique de brossage adaptée, associée à l’utilisation de brossettes interdentaires, de fil dentaire et, si besoin, de bains de bouche spécifiques, permet de réduire significativement la charge bactérienne. En complément, les interventions professionnelles comme le détartrage ou le débridement radiculaire offrent un nettoyage en profondeur impossible à réaliser à domicile. Comment orchestrer ces différentes approches pour obtenir une véritable décontamination buccale tout en respectant la flore bénéfique ?
Méthode de bass et technique de stillman pour le brossage optimal
Les techniques de brossage de Bass et de Stillman sont parmi les plus recommandées pour optimiser l’élimination de la plaque dentaire tout en préservant les tissus gingivaux. La méthode de Bass modifiée consiste à placer la brosse à dents à un angle de 45° par rapport au sillon gingivo-dentaire, puis à effectuer de petits mouvements vibratoires et rotatifs. Cette gestuelle permet de déloger la plaque située à la jonction entre la dent et la gencive, là où se forment les premières lésions carieuses et les gingivites.
La technique de Stillman, quant à elle, est particulièrement indiquée chez les patients présentant une récession gingivale ou une hypersensibilité cervicale. La brosse est positionnée également à 45°, mais sur la gencive attachée, puis déplacée de manière roulée vers l’incisal ou l’occlusal. Ce mouvement massage-décapage stimule la circulation sanguine gingivale et favorise la santé des tissus, tout en nettoyant les collets dentaires. Dans les deux cas, l’utilisation d’une brosse à poils souples et un temps de brossage d’au moins deux minutes, deux fois par jour, sont essentiels pour un contrôle optimal de la plaque.
Irrigation subgingivale avec solution de chlorhexidine 0,12%
L’irrigation subgingivale à la chlorhexidine 0,12 % constitue une approche chimique ciblée pour réduire la charge bactérienne dans les poches parodontales. À l’aide d’une canule souple ou d’un hydropulseur muni d’une embout spécifique, la solution est délivrée directement sous le rebord gingival, au plus près des colonies bactériennes anaérobies. Cette diffusion locale permet d’atteindre des zones inaccessibles au brossage ou au simple rinçage, en particulier chez les patients présentant une parodontite modérée à sévère.
La chlorhexidine est considérée comme le « gold standard » des antiseptiques buccaux en raison de son large spectre antibactérien et de sa substantivité, c’est-à-dire sa capacité à se fixer sur les tissus buccaux et à se relarguer progressivement. Cependant, son utilisation doit rester limitée dans le temps (généralement 2 à 3 semaines) afin d’éviter des effets indésirables tels que coloration des dents, altération du goût ou perturbation excessive du microbiote. L’irrigation subgingivale s’intègre donc dans un protocole de décontamination encadré par le praticien, en complément des soins mécaniques professionnels.
Détartrage ultrasonique et débridement radiculaire
Le détartrage ultrasonique est l’un des piliers de la décontamination professionnelle de la cavité buccale. Les inserts ultrasoniques vibrent à haute fréquence, fragmentant le tartre supra- et sous-gingival et rompant l’architecture du biofilm sans endommager l’émail lorsque le geste est bien maîtrisé. Cette procédure permet de réduire significativement la quantité de bactéries pathogènes, notamment les anaérobies impliquées dans les parodontites et l’halitose, et de lisser les surfaces dentaires, limitant ainsi la ré-adhésion rapide de la plaque.
En cas d’atteinte parodontale plus avancée, le débridement radiculaire (ou surfaçage radiculaire) devient nécessaire. À l’aide de curettes manuelles ou d’inserts spécifiques, le praticien élimine le tartre adhérent et le ciment radiculaire infecté, puis polit la surface de la racine. Ce lissage favorise la réattache des fibres gingivales et la réduction de la profondeur des poches. Bien que parfois inconfortables, ces interventions sont déterminantes pour assainir durablement l’environnement sous-gingival et stabiliser la maladie parodontale.
Bains de bouche au fluorure stanneux et peroxyde d’hydrogène
Les bains de bouche au fluorure stanneux occupent une place particulière dans la prévention des caries et des gingivites. Le fluorure stanneux combine un effet reminéralisant sur l’émail et une action antibactérienne ciblée sur les bactéries cariogènes comme Streptococcus mutans. En renforçant la structure cristalline de l’émail et en limitant la production d’acides, il contribue à rendre les dents plus résistantes aux attaques acides répétées, notamment chez les patients à risque carieux élevé.
Le peroxyde d’hydrogène, utilisé à faible concentration dans certains bains de bouche, exerce une action oxydante qui déstabilise les membranes bactériennes et éclaire la coloration superficielle des dents. Ce type de produit peut être utile en cures courtes pour diminuer la charge bactérienne et améliorer l’esthétique, mais il doit être manié avec prudence pour ne pas irriter les muqueuses ni perturber excessivement le microbiote oral. L’idéal est de réserver ces solutions à des indications précises, sous conseil professionnel, et de ne jamais les considérer comme un substitut au brossage mécanique.
Protocoles d’hygiène bucco-dentaire préventive personnalisée
Un protocole d’hygiène bucco-dentaire efficace ne peut être réellement protecteur que s’il est adapté à votre profil bactérien, à vos habitudes alimentaires et à vos antécédents médicaux. Les recommandations standard (brossage biquotidien, fil dentaire, visites annuelles) constituent une base, mais ne suffisent pas toujours pour prévenir les infections orales chez les patients à risque. L’objectif d’une approche personnalisée est de transformer ces recommandations générales en un plan de soins sur mesure, ajusté à la fois à votre microbiote et à votre mode de vie.
La première étape consiste en un bilan bucco-dentaire complet, incluant un examen clinique, un dépistage des lésions carieuses et parodontales, et, lorsque nécessaire, des analyses microbiologiques ciblées. À partir de ces données, le praticien définit une « carte de risque » intégrant le risque carieux, le risque parodontal et le risque d’halitose. Sur cette base, il devient possible de moduler la fréquence des consultations, le type d’outils d’hygiène à utiliser et la nécessité éventuelle de traitements adjuvants comme les probiotiques oraux ou les gels fluorés concentrés.
Nutrition thérapeutique et immunomodulation salivaire
La nutrition joue un rôle déterminant dans la protection de la cavité buccale contre les bactéries pathogènes, au même titre que l’hygiène mécanique. Une alimentation riche en sucres simples et en aliments ultra-transformés nourrit préférentiellement les bactéries acidogènes et favorise la formation de biofilms cariogènes. À l’inverse, une diète abondante en fibres, en légumes verts et en protéines de qualité stimule la mastication, augmente le flux salivaire et soutient les défenses naturelles de la bouche. La salive, véritable « sérum physiologique » de la cavité buccale, contient des enzymes, des immunoglobulines et des peptides antimicrobiens qui participent activement à l’immunité orale.
Certains nutriments exercent une action particulièrement intéressante sur l’immunomodulation salivaire. La vitamine D et les oméga-3, par exemple, contribuent à réguler l’inflammation gingivale et à renforcer la réponse immunitaire locale. Les polyphénols présents dans le thé vert, le cacao brut ou certaines baies possèdent des propriétés antibactériennes et anti-adhésives vis-à-vis de S. mutans et d’autres pathogènes oraux. Enfin, l’intégration de probiotiques spécifiques (comme Lactobacillus reuteri ou Streptococcus salivarius K12) dans une stratégie de nutrition thérapeutique peut aider à recoloniser la bouche avec des bactéries protectrices. En combinant ces leviers alimentaires à une bonne hydratation et à la limitation des grignotages sucrés, vous offrez à votre microbiote buccal un environnement favorable à l’équilibre.
Technologies antibactériennes innovantes et photothérapie dynamique
Les avancées récentes en odontologie ont vu émerger des technologies antibactériennes innovantes, visant à cibler plus finement les bactéries pathogènes tout en préservant le microbiote bénéfique. Parmi elles, la photothérapie dynamique (PDT) suscite un intérêt croissant dans le traitement des maladies parodontales et des infections résistantes. Le principe est comparable à celui d’un « cheval de Troie lumineux » : un photosensibilisant est appliqué sur la zone infectée, puis activé par une lumière d’une longueur d’onde spécifique. Cette activation génère des espèces réactives de l’oxygène qui détruisent sélectivement les cellules bactériennes.
La PDT présente l’avantage de ne pas induire de résistance bactérienne et de pouvoir être répétée sans altérer les tissus environnants, contrairement à certains antiseptiques agressifs. Elle s’intègre souvent en complément d’un débridement mécanique, pour potentialiser l’élimination des pathogènes dans les poches parodontales profondes ou autour des implants. D’autres technologies, comme les lasers de faible énergie, les revêtements antibactériens sur les restaurations dentaires ou les dispositifs à libération contrôlée d’antimicrobiens, complètent cet arsenal thérapeutique. En combinant ces outils de pointe à une hygiène quotidienne rigoureuse et à une alimentation protectrice, il devient possible de maintenir un microbiote buccal équilibré et de protéger durablement la cavité buccale des bactéries les plus agressives.